摘要
在全球面對人口老齡化挑戰之際,深入了解當前老齡化研究的關鍵趨勢顯得尤為重要,以便應對未來的健康需求。 歸納要點:
- AI驅動的多組學整合與動態模型建構,能更精準地預測個體生物年齡,並模擬不同干預措施對衰老的影響。
- 表觀遺傳時鐘提供了校準生物年齡的新方法,研究者正探索如何透過特定酶的調控來改善健康狀況。
- 液態活檢技術使得非侵入性監測細胞衰老成為可能,有助於早期診斷與治療效果追蹤。
AI與系統生物學:解鎖長壽與精準抗衰老的未來
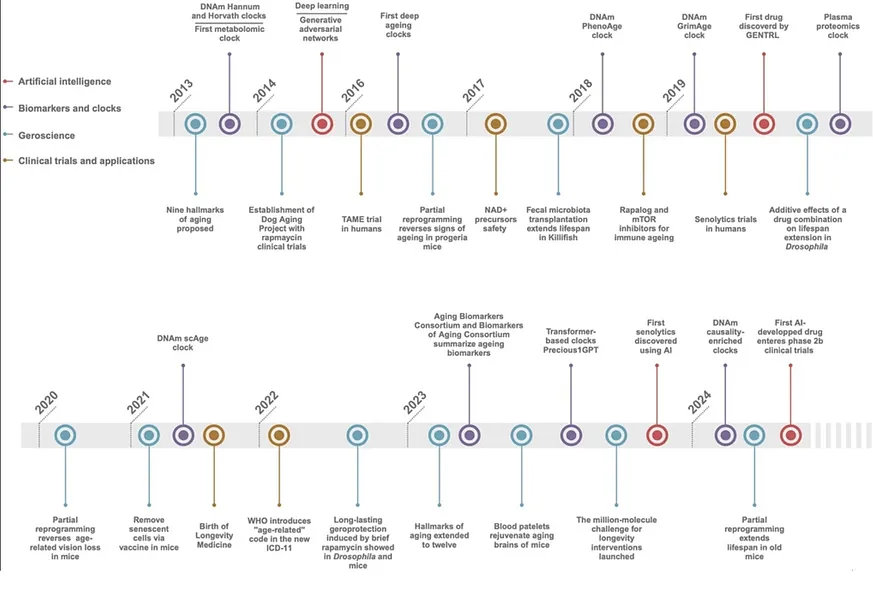
在過去十年中,衰老研究已經從基礎的生物學研究轉變為一個高度技術化和多學科的領域。這一變革始於2013年提出的九大衰老標誌,以及2023年擴充套件至十二大衰老標誌,背後驅動因素不僅包括生物學上的諸多進展,也受到科技創新的影響,尤其是人工智慧(AI)的發展,使得更為複雜的生物標記物發現及臨床幹預成為可能。以下,我將根據2023年衰老研究與藥物發現會議(ARDD)期間發布的一篇綜合文章《長壽生技:橋接AI、生物標記、衰老科學與健康長壽的臨床應用》來強調一些塑造這一領域的重要趨勢。1. **AI驅動的精準衰老幹預:超越生物標記物發現,邁向個人化治療策略。** 典型查詢意圖包含:「個人化抗衰老療法」、「AI輔助衰老幹預」、「多組學整合分析於衰老研究」等。該文章中提及的AI應用已不再侷限於生物標記物的發現,例如利用深度學習模型識別與衰老相關的基因表達模式或從影像資料中預測生物年齡,而是進一步發展出個人化治療策略。這些策略包括:(a) 基於多組學資料(如基因組學、蛋白質組學、代謝組學等)的整合分析,以建立更精確的衰老風險評估模型,實現「預測性醫學」;(b) AI驅動的藥物篩選和再利用,加速針對特定衰老途徑的藥物研發並縮短臨床試驗週期;(c) 利用AI最佳化治療方案,根據個體基因組、生活方式及環境因素制定個性化幹預方案,以最大限度提高療效並降低副作用。例如,AI可以根據患者特定基因型預測其對某種抗衰老藥物反應,使之更具針對性。此趨勢將使抗衰老研究從「群體平均」模式轉向「個體差異」精準醫學模式,大幅提升治療效果與效率。
2. **衰老研究系統生物學整合與網路藥理學應用:從單一通路到複雜網路系統性的理解。** 典型查詢意圖包含:「衰老網路藥理學」、「系統生物學與衰老」、「多靶點抗衰老藥物」等。在過去,許多關於衰 aging 的研究常聚焦於單一通路,如端粒縮短或線粒體功能障礙,但《長壽生技》文章強調了系統生物學在理解這些複雜性方面的重要性。(a) 構建全面性的幫助文獻回顧和未來方向指引,使各種不同路徑和機制相互對映並形成完整框架; (b) 網路藥理學能夠協助設計涵蓋多靶點的新型藥品,提高療效並減少耐藥性的產生,相較於單靶點藥品,多靶點藥品能夠更有效應對複雜情況;(c) 整合「omics」資料以識別關鍵網路節點與調控機制,為新型抗aging 藥品開發提供精準目標。這將引領抗-aging 藥品研發進入一個嶄新時代。因此,在未來,我們不僅會看到技術進步,還可能見證醫學上變革性的突破,有望實現真正意義上的健康長壽。
我們在研究許多文章後,彙整重點如下
- AI技術可應用於醫學,幫助科學家開發更有效的抗衰老療法。
- 新診斷技術結合生物標誌物與AI,提高了衰老速度的預測準確性。
- APPAM平台開發出多種抗衰老藥物和治療方法,包括細胞和基因治療。
- Insilico的PandaOmics軟體能預測針對衰老及相關疾病的新藥分子靶點。
- 運動介入計畫結合AI已顯著改善高齡者健康狀況,提升運動效果。
- 蘇格蘭愛丁堡大學研究團隊利用AI尋找有效抗衰老藥物,並發現中藥成分具潛力。
隨著科技進步,特別是人工智慧在醫學領域的應用,我們對抗衰老有了新的希望。透過智能化診斷與治療方案,不僅能提供更精準的預測,也能研發出多元化的抗衰老藥物。這些創新不僅限於西醫,中醫也被納入考量,讓人期待未來能夠實現中西醫融合,共同延緩衰老、增進健康。如果你也關心自己的健康與長壽,不妨留意這些前沿研究帶來的好消息!
抗衰老新發現:超越「媽媽的建議」,個人化延緩老化的方法
我也想分享一些關於今天對「普通人」能做些什麼的看法。我最近才接觸到衰老研究這個領域,當我在八月底首次參加位於哥本哈根舉辦的第十一屆衰老研究與藥物發現會議(ARDD2024)時,獲得了這樣的機會。這次體驗非常愉快,無論是在組織上還是內容上,但這篇文章並不是要討論那一點。我發現衰老研究產業潛力巨大,有許多不同的介入策略正在進行前臨床階段、動物模型實驗的成功,甚至還有一些與衰老相關的臨床試驗正在進行。我留下的印象是,目前似乎除了傳統的「好好睡覺、吃得健康、運動、每年檢查一次身體和社互動動」等建議之外,對一般大眾可用的方法不多(也就是「媽媽告訴你的事」)。
目前的衰老研究已不再僅限於宏觀層面的生活方式建議。尖端感測器技術的發展,例如可穿戴式裝置監測生物標記(如端粒長度、炎症標記物、腸道菌群組成等)的變化,使得個人化衰老評估成為可能。這使我們能超越傳統「睡好、吃好、動好」的普世建議,轉向更精準的個人化幹預。例如,可以根據個人的生物標記資料制定針對性的營養補充策略(如針對特定代謝途徑的補充劑)、運動計劃(例如基於基因表現型設計的訓練強度)或生活方式調整,以最大程度地延緩衰老速度並降低與年齡相關疾病風險。
在ARDD2024會議中展現了許多單一干預措施在動物模型上的成功,但真正突破可能在於開發多靶點和組合療法。目前許多研究正探索不同介入策略之間協同作用,例如將雷帕黴素(mTOR抑制劑)和NAD+前體(如煙醯胺核糖)或抗氧化劑結合,以達到更強效抗衰老效果。「藥物再定位」策略也備受矚目,此方法重新評估已獲批藥物在抗衰老方面的新潛力。例如,一些原本用以治療其他疾病的藥物,在研究中顯示出延緩衰老或改善與年齡相關疾病表型之潛力。這些發現將為臨床試驗提供新方向,同時縮短藥物研發週期。
頂尖專家需要深入評估這些組合療法或藥物再定位策略所可能帶來的副作用及相互作用,以及其長期安全性,因此開發嚴謹且有效果良好的臨床試驗設計至關重要,以確認它們是否安全有效。最終目的是實現更有效、更安全的大眾抗老幹預策略。
AI驅動的精準抗老:多組學分析與個人化醫療的未來
有一些例外情況,對於擁有足夠領域知識的人來說,還是有幾種潛在的有益療法可以選擇,以便真正理解和管理風險與效益之比。雖然結果尚未得到明確證實,但很可能是如此。因此,我們正處於每個人都能實現長壽的初期階段,但同時也可以期待一些重大進展會在不久的將來出現,或許還會帶來意想不到的驚喜(誰又能確定呢?)。無論如何,讓我們深入探討一下:機器學習演算法、深度學習技術以及大規模資料分析的整合,使得老化生物標記研究得以識別和驗證這些生物標記,它們對於診斷疾病、預測結果並量身定製治療方案至關重要。例如,應用深度學習技術分析各種組織細胞影象後發現,核形態是一個新的通用細胞衰老標記。僅依賴單一生物標記通常不足以準確追蹤老化過程。相反地,更全面的方法是使用生物標記面板或綜合生物標記,它們結合了多種“組學”技術(如基因組學、蛋白質組學及代謝組學)的資料。
**專案1:多組學整合與AI驅動的動態老化生物標記網路 (Dynamic Aging Biomarker Network driven by Multi-omics Integration and AI):** 延續原文提及的多組學整合策略,頂尖專家更需關注的是將這些資料動態地整合建模,而非僅僅停留在靜態的生物標記面板。這需要借助更先進的AI技術,例如圖神經網路(Graph Neural Networks, GNNs)或動態貝葉斯網路(Dynamic Bayesian Networks, DBNs),來建立一個能反映個體老化過程的動態網路。此網路中的節點代表不同的生物標記,而邊則代表它們之間複雜相互作用和動態變化。這樣的模型能精準預測老化速度、疾病風險,以及個人化幹預措施有效性。
**專案2:老化幹預策略的個人化及可解釋性AI模型 (Personalized and Explainable AI Models for Aging Intervention Strategies):** 原文提到「風險效益比」,而這正是個人化醫學核心所在。未來發展方向不僅限於發現新的生物標記,更重要的是利用AI模型將這些生物標記與個體化老化幹預策略相結合。單純的預測模型不足以令人信服,因此頂尖專家更加重視模型可解釋性(Explainability)。為此,需要發展更先進可解釋AI技術,例如SHAP值(SHapley Additive exPlanations)或者LIME(Local Interpretable Model-agnostic Explanations),以解釋AI模型預測結果並揭示哪些生物標記或其組合對於老化幹預效果產生了關鍵影響。例如,一個可解釋AI模型可以說明為什麼某種特定幹預方案對某位個體有效,而對另一位則無效,從而實現真正意義上的個人化醫療。此專案的研究也將推動建立更嚴謹臨床試驗設計,以驗證這些個人化幹預策略之有效性和安全性。
我們仍處於探索最有效率且具突破性的長壽科技早期階段,但未來卻充滿希望與可能性。
使用可解釋的人工智慧在開發利用非侵入性技術預測年齡的模型中至關重要。未來,人工智慧與單細胞測序和空間轉錄組學等先進技術的結合,可能會推動生物標記物的發現,特別是對於複雜的多因素疾病而言。值得注意的是,目前焦點正逐漸轉向識別治療性生物標記物,這些標記物不僅能預測與年齡相關疾病的發作,也能追蹤對抗老化治療(gerotherapeutic interventions)的反應——這類治療旨在延緩、預防或減輕與老化相關的病症,同時延長健康壽命。
AI加速藥物發現:攻克衰老與年齡相關疾病的網路藥理學新策略
像 Insilico Medicine、BioAge Labs 和 Deep Longevity 等公司,正將人工智慧(AI)整合進藥物發現和診斷過程中,並特別考慮衰老過程。他們的研究重點在於理解影響長壽的基因和表觀遺傳機制。這些工作的核心在於展示 AI 在加速藥物發現過程中的潛力,透過快速的計算模擬測試化合物,再轉向實驗室試驗。例如,Insilico Medicine 成功建立了一個臨床候選藥物的管道,其從概念到臨床前候選者提名的平均時間約為 18 個月。這一時間表並非傳統研究模式所能比擬,而我大約一年前在分析十個 AI 藥物發現平台時也談到了這一案例。需要指出的是,Insilico Medicine 的管道中,大多數藥物候選者其實並非針對衰老幹預,而是針對廣泛的與年齡相關疾病,如纖維化等,有著潛在與衰老研究相關的新靶點。在現代醫學分類中,衰老被認為不是一種疾病,因此即使其研究可能與衰老過程高度相關,也難以圍繞抗衰老目標建立一家臨床階段公司。
**AI 驅動的衰老幹預藥物研發:超越單一疾病靶點的網路藥理學應用**:目前 Insilico Medicine 等公司雖聚焦於與年齡相關疾病(如纖維化),但其 AI 平台真正的潛力在於網路藥理學應用。頂尖專家需要關注的是,AI 是否能超越單一靶點限制,建立更全面的衰老相關基因網路模型。這將允許更精準地預測藥物對多個衰老途徑的影響,以開發出具有多重靶點作用而非僅針對單一疾病的藥物。此過程需整合多組學資料(如基因組學、轉錄組學、蛋白組學等),搭配更精細化的 AI 模型,例如圖神經網路 (Graph Neural Networks) 或深度強化學習 (Deep Reinforcement Learning),來最佳化藥物設計及預測其對複雜衰老網路之整體影響。這無疑是超越當前「圍繞年齡相關疾病」策略的一項關鍵突破,更接近於幹預衰老過程之根本目標。
**AI 模型可解釋性和可信度:提升臨床試驗可預測性與監管透過率**:儘管 Insilico Medicine 縮短了藥物研發時間,但 AI 模型的可解釋性仍然是阻礙其廣泛應用和監管透過的重要瓶頸。頂尖專家的關鍵在於深入理解 AI 模型如何做出預測,以及如何量化其不確定性。不僅涉及科學嚴謹性,也直接影響臨床試驗成功率及監管機構信任。因此未來研究需集中於開發具有更高可解釋性的 AI 模型(例如規則驅動模型、LIME 或 SHAP 解釋方法),並結合傳統藥物研發知識來驗證 AI 模型之預測。需要建立完善資料質量控制及驗證機制,以確保 AI 模型之可靠性。
破解老化之謎:精準醫療與資料共享的雙重策略
當我在 ARDD2024 的一場座談會上詢問有關老化研究領域的公司應如何建立發展管道時,得到的答案相當出乎意料。我沒有錄下那個回答,但如果我記得沒錯的話,Alex Zhavoronkov 說,其實這件事相當困難,因此有志於老化領域的新型生技公司應該朝著「合法疾病」的方向努力,以便將其商業化,包括結構化臨床試驗等。但他們也應該嘗試發現與老化過程高度相關的新穎且廣泛的目標。這樣一來,一方面,他們可以透過像其他人一樣遵循標準臨床監管途徑而擁有清晰的路徑(因此能吸引投資並制定可理解的商業里程碑),另一方面,他們也會積累關於老化過程的新知識和專業技能,以便在產業對老化研究作為疾病有明確路徑時佔據優勢。一、 **突破「老化」定義的臨床試驗設計:** Zhavoronkov 教授指出了老化研究中的關鍵瓶頸:缺乏明確的疾病定義與標準臨界途徑。目前業界正積極探索將老化視為多因素疾病,而非單一病症,這意味著臨床試驗設計需要跳脫傳統框架,例如採用多組學整合分析(整合基因組、蛋白質組、代謝組等資料),以更全面地評估幹預措施對於老化影響。研究者開始重視「健康老化」指標,如生物年齡、生理功能等,而不僅依賴死亡率或特定疾病發病率來作為主要評估終點。此舉需要開發更精密的生物標記及評估工具,例如基於 AI 的影像分析技術,以及靈敏度更高的生理功能評估方法,以捕捉幹預措施對個體健康壽命之影響。策略成敗取決於科學界是否能達成共識,制定客觀且全面性的「老化」定義及評估標準,進而建立科學而可行的臨床試驗架構,使投資者能獲得可預測商業模式。這也呼應了教授建議先攻克合法疾病策略,即從可量測指標切入,逐步累積資料和經驗,以奠定日後針對「老化」本身進行研究之基礎。
二、 **跨領域合作及資料共享平台建設:** 老化研究複雜性要求跨領域專業知識與技術,包括基因組學、蛋白質組學等。目前各領域間資料共享及協作仍顯不足。因此,建立安全可靠且標準化的平台至關重要。此平台不僅需整合不同機構資料,也要促進資料分析方法標準,提高成果可信度。平台還需支援多種資料型別,包括基因組、影像和臨床資料,同時提供有效分析工具方便研究者挖掘資料。如果再加上人工智慧技術如機器學習和深度學習,可望快速找出新的相關標記物和治療靶點,加速研發程序。在此背景下,此類資料共享平台將大幅提升效率與品質,也為新興生技公司提供可靠支援,降低風險並推動產業蓬勃發展。因此,可以說Zhavoronkov教授所倡導聚焦特定疾病以累積經驗與資料,在未來建立有效分享網路上形成良性迴圈,是非常符合趨勢的重要思考方向。
AI與多組學資料整合:解碼生物年齡,實現個人化抗衰老
生物標記的發現——可測量的生物過程指標——對於老化研究起到了重要作用。這些生物標記使得我們能夠追蹤生物老化,這與時間上的老化是不同的。自從2013年Steve Horvath開發出首個DNA甲基化時鐘以來,在建立更為精細的老化時鐘方面已取得了顯著進展,這些新型時計整合了各種組學資料(例如:基因組、蛋白質組、代謝組)。例如,在2023年推出的OMICmAge時鐘,融合了來自蛋白質組、代謝組、臨床資訊和DNA甲基化的資料,以預測疾病風險和壽命。此時鐘在預測5年和10年的存活率方面,比早期版本顯示出了更高的準確性。像Biolearn、Clockbase和methylCIPHER等平台專注於老化生物標記的開發和驗證,為研究人員提供了標準化的資料集及比較現有生物標記所需的基準。這種標準化對於將生物標記從研究實驗室轉向臨床應用至關重要。
**一、多組學整合與人工智慧的深度融合:超越單一生物標記的侷限性** 目前雖然多組學整合的生物老化時鐘,例如OMICmAge,已經展現出比單一組學指標(例如僅DNA甲基化)更佳的預測能力,但其預測準確度仍有進步空間。頂尖研究者正積極探索將人工智慧,尤其是深度學習技術,更深入地整合到生物老化時鐘的建構中。這不僅能更有效率地處理和分析海量多組學資料(包含基因組、蛋白質組、代謝組、轉錄組等),還能夠挖掘出單純依靠統計模型無法發現的複雜生物老化機制中的非線性關係與互動作用。例如藉由深度學習模型,可以自動識別不同生物標記之間協同或拮抗作用,進而構建更精準、更具解釋性的老化時鐘模型。未來,希望這些老化時計不再僅是一個預測工具,而是能深入闡釋老化過程並揭示其機制的平台。
**二、動態生物標記與個人化老化幹預:從靜態測量到持續監控** 現有的大多數生物老化時鐘都是基於一次樣本測量,因此提供的是相對靜態的一個生命年齡估計。由於生活方式、環境因素以及疾病影響,實際上,生物老化是一個動態過程,其速度和軌跡會隨時間變遷。因此未來研究重點將轉向開發及應用**動態生物標記**,即那些可以持續監控並追蹤人的生命程序的新指標。這需要結合可穿戴裝置與液體活檢等技術,實現對這些標記長期且實時監測,透過動態監測,我們將能夠更加精準地評估個體衰老人速與軌跡,並據此制定個性 化干預策略。例如,對特定標記變化作出適時調整,比如生活方式或營養攝入,從而延緩衰減速度並降低疾病風險。這將推動精準醫學在抗衰領域應用,使真正意義上的個性 化管理成為可能。
破解長壽密碼:從基因到表觀遺傳的衰老研究新突破
如同我在引言中提到的,衰老研究已發展出十二項衰老標誌,其中包括分子損傷(例如基因組不穩定性、端粒縮短)以及細胞過程(例如自噬、蛋白質恆常性)。這些透過廣泛研究所識別的標誌,提供了理解衰老如何在分子、細胞及系統層面上表現的全面框架。以基因組不穩定性的研究為例,它強調了累積的DNA損傷和端粒縮短是衰老的重要驅動因素。來自Ercc1突變小鼠——一種早衰綜合症模型——的顯著研究顯示,特定的DNA修復基因突變能加速衰老過程,引發其他衰老標誌,例如細胞老化和炎症。當代對於衰老研究的方法論也有所突破,不再僅限於單一層面的探討,而是積極整合多組學資料,包括基因組學、轉錄組學、蛋白質組學及代謝組學等,並結合單細胞分析技術,使得研究者可以更精確地追蹤不同細胞型別在衰老過程中的異質性變化。例如,單細胞RNA測序能揭示不同細胞群體中與衰老相關基因表達的差異,有助於釐清哪些細胞型別對於衰老影響最大,以及它們之間相互作用如何影響整體年齡程序。這種方法超越了傳統對單一基因或途徑的關注,提供了一個更全面的機制圖譜,有助於開發更具針對性的幹預策略。
進一步而言,多組學資料與單細胞分析技術的結合,再加上如空間轉錄組學等新興技術,可以更加深入地解析衰老在空間上的異質性,比如不同細胞型別之間在特定微環境中的互動作用如何推動區域性衰老程序。這樣的方法對於理解複雜疾病與年齡之間的關聯至關重要,例如探究某些特定組織中衰老細胞累積如何促成癌症發生。
在探索表觀遺傳學修飾方面,我們也看到新的進展。儘管原文提及了基因組不穩定性,但表觀遺傳修飾(如DNA甲基化、組蛋白修飾及非編碼RNA)也在年齡增長中扮演著關鍵角色。近年的研究指出,一些表觀遺傳修飾酶隨著年齡改變其活性,導致基因表達模式紊亂,加速了衰老過程。因此,針對這些修飾所採取的一系列創新幹預策略,如使用藥物抑制特定表觀遺傳酶活性或透過飲食調節來影響DNA甲基化模式,也正受到重視。一些初步結果顯示補充葉酸或B族維他命可能會延緩該過程,但這仍需更多實證支援。
透過提升表觀遺傳時鐘的準確度,我們希望能有更精確的方法來評估生物年齡,以此輔助未來臨床應用和深入了解複雜且多面向的生命科學議題。」
抗衰老療法新突破:表觀遺傳、自噬與液態活檢的整合應用
表觀遺傳修飾已成為另一個關鍵的特徵。近期在部分重程式設計方面的進展——即暫時使用Yamanaka因子將細胞重置至更年輕狀態——顯示出逆轉與年齡相關損傷的潛力。這種方法也伴隨著風險,例如可能破壞細胞身份或增加癌症風險,因此在治療應用中需要謹慎施用。在自噬(細胞回收過程)領域,人工智慧(AI)已被用來識別針對線粒體自噬(mitophagy,即選擇性降解線粒體)的潛在藥物候選者,並在阿茲海默病的前臨床模型中顯示出有希望的結果。細胞衰老是指當細胞停止分裂並釋放促炎因子,這一過程在衰老中扮演著舉足輕重的角色。移除這些衰老細胞已成為抗衰老療法的一個主要目標。專門設計用於選擇性消除衰老細胞的一類藥物——Senolytics,在前臨床和早期臨床研究中顯示了良好的前景。**表觀遺傳修飾與液態活檢的整合應用:** 現有研究主要著重於表觀遺傳修飾在細胞衰老中的作用,例如DNA甲基化模式的改變。單靠分析細胞或組織樣本中的表觀遺傳變化難以準確反映全身性衰老程度及個體差異。未來研究方向將聚焦於整合液態活檢技術,透過分析血液或其他體液中的外泌體、迴圈腫瘤DNA以及遊離DNA中攜帶的表觀遺傳標記,更精準、非侵入性地監控個體整體老化程序及評估部分重程式設計療法或Senolytics療法的有效性,此舉有望突破現有研究限制,更精確地制定抗衰老治療策略。
**自噬與細胞衰老之間互作機制及治療靶點開發:** 目前研究多集中於單一治療靶點,如促進自噬或清除衰老細胞,但事實上,自噬與細胞衰老之間存在複雜相互作用。未來必須深入探討兩者之間的分子機制,比如如何調節自噬相關基因表達,以及自噬效率降低如何影響SASP(衰老人群所分泌之炎症因子)的產生。因此,更精確的治療策略應同時調節自噬和細胞衰老,如研發同時針對PINK1/Parkin途徑和SA-β-gal標記物的新型雙重作用藥物,以更有效延緩 aging。AI技術亦可被運用於預測和篩選藥物組合,加快新藥研發步伐,而這需要跨學科合作結合不同專家的知識,共同建立更為精密且具預測性的疾病模型,以考量不同器官組織差異及疾病異質性。
延緩老化:精準醫療與創新療法如何逆轉衰老
Dasatinib(達沙替尼,一種抗癌藥物)和Quercetin(槲皮素,一種天然化合物)是最早顯示出在動物模型中減少衰老標記並改善健康狀態的senolytics(去衰老劑)。Unity Biotechnology是一家由Nathanial ′Ned′ David創立的公司,專注於針對眼部疾病的senolytic藥物開發,並已經展開針對老化相關疾病的臨床試驗,以透過清除衰老細胞來改善健康。其他創新方法包括senomorphics,這類技術透過調節衰老細胞的行為而不將其殺死,以及利用細胞外囊泡(Extracellular Vesicles, EVs)和CAR-T療法來移除或重生衰老細胞。目前這些技術正在積極研究中,以確定其在人類中的安全性與有效性,尤其是在治療慢性與年齡相關疾病方面的潛力。對於線粒體功能障礙及營養感應途徑的研究揭示了這些系統在調節衰老過程中的關鍵角色。線粒體功能障礙會導致能量生成減少及氧化壓力增加,進而引發細胞損傷。因此,針對線粒體健康的治療幹預措施,例如NAD+前驅物及天然化合物trigonelline等,被探索以期恢復線粒體功能。
**1. Senolytic藥物開發的精準度與個人化醫療:** 現階段的senolytic研究雖然Dasatinib和Quercetin等藥物展現初步成效,但其作用機制複雜,而不同個體及器官組織間存在巨大的差異。因此未來senolytic藥物開發需著重於精準標靶,包括:(a) **更深入的衰老細胞異質性研究**:需更仔細地區分不同型別之衰老細胞及其特有標記,進而研發高效且低毒性的特定亞群藥物;(b) **生物資訊學與AI輔助藥物篩選**:利用大資料分析、基因組學、蛋白質組學及代謝組學整合資料,以預測藥物靶點,加速新候選senolytic藥品篩選;(c) **個體化治療策略**:結合基因檢測、影像檢查以及臨床資料制定個別化治療方案,使患者獲得最有效之用藥組合。
**2. Senomorphics與EVs 的協同作用及臨床轉化:** 雖然senomorphics和EVs各具潛力,但若能結合應用可能產生協同增效效果,大幅提升抗衰老效果。(a) **Senomorphics可作為EVs調控工具**: 特定senomorphics可調節衰老細胞所分泌EVs內容,使之具有更新或修復功能,而非持續釋放促炎因子;(b) **工程化EVs靶向清除衰老細胞**: 可設計改造EVs攜帶senolytic藥品或siRNA,可精準靶向消除受影響之成熟或病變細胞。同時運載再生修復相關分子以促進組織修復;(c) **臨床轉化途徑探索**: 目前涉及到senomorphics和EVs的新興療法仍處於早期階段,需要設計更嚴謹之臨床試驗以評估安全性與有效性。也需要探索此技術與其他抗衰手段如NAD+補充療法、飲食幹預等相互配合才能實現真正意義上的臨床轉換。
以上探討不僅為我們理解抗衰退機制提供了新的視角,也指引著未來可能實現的一系列突破,有望推動抗 aging 研究邁入全新境界。
mTOR 和 AMPK 通路是控制細胞對營養水平反應的重要機制,同時也與老化過程密切相關。研究顯示,像雷帕黴素(rapamycin)這類藥物透過抑制 mTOR,能夠延長壽命,因為它減少了蛋白質合成並促進自噬。二型糖尿病藥物美託洛(metformin)也被重新利用來針對老化,其在營養感知和代謝方面的作用備受關注。目前正在進行的 TAME(Targeting Aging with Metformin)試驗,由尼爾·巴爾齊萊博士(Dr. Nir Barzilai)主導,旨在驗證美託洛是否能延長人類壽命並延緩與年齡有關的疾病。
AI驅動的精準抗衰老:多組學整合與個人化治療的未來
儘管實驗室技術已有顯著進展,但臨床轉化仍然是衰老研究中最具挑戰性的方面之一。從發現到臨床應用的過程需要對生物標記物進行嚴格的驗證和統一,並克服各種法規障礙。像 Biolearn、Estimage 和 Clockbase 等倡議旨在透過提供標準化指標和衰老生物標記物的驗證平台來促進這一過程。在臨床設定中,針對衰老機制而設計的治療——即 gerotherapeutics 受到越來越多的關注。目前許多臨床試驗專注於針對拮抗性特徵(如營養感知失調和線粒體功能障礙)的介入,因為這些過程在前期研究中已顯示出最大的潛力。**專案1:多組學整合與人工智慧在衰老生物標記物驗證及臨床轉化中的應用** 儘管 Biolearn、Estimage 和 Clockbase 等倡議提供了標準化指標和驗證平台,但單一組學資料的侷限性依然存在。頂尖專家們正積極探索多組學整合策略,例如結合基因組學、轉錄組學、蛋白質組學和代謝組學資料,利用人工智慧技術(如機器學習、深度學習)建立更精確、更具預測性的衰老生物標記物模型。此方法不僅能提升生物標記物的驗證效力,更能從海量資料中挖掘潛在的治療靶點,加速臨床轉化過程。例如,利用深度學習模型分析多組學資料,可以識別出與特定衰老表型高度相關的基因表達模式或蛋白質修飾,從而精準地篩選出潛在藥物靶點,並預測藥物療效及副作用,有效降低臨床試驗風險與成本。
**專案2:衰老幹預的個體化治療策略與動態監測** 目前臨床試驗主要集中於針對衰老拮抗性特徵(例如營養感知失調和線粒體功能障礙)的幹預,但往往忽略了衰老本身所具備的異質性。頂尖專家們致力於發展個體化治療策略,以考量年齡、遺傳背景、生活方式及疾病史等因素,制定更精確且有效的幹預方案。這需要結合多組學資料,以建立個體化衰老風險評估模型,並根據每位患者獨特的衰老特徵選擇最佳介入措施。即時監控個體對幹預措施反應的重要性亦愈加凸顯。透過可穿戴裝置及遠端監測技術持續收集生理指標和生物標記資料,可以實時追蹤治療效果並迅速調整方案。因此,需要開發更敏感且專門化的新型生物標記,以便提供更便捷、更經濟有效之監測技術。
未來研究將重點放在發展綜合多組學資料、人工智慧技術及動態監測系統之個體化管理平台,以實現精準防範及治療真正延緩衰老,提高高齡者生活品質。
延緩衰老:個人化醫療與未來健康策略
延壽醫療的出現代表著從傳統以疾病為中心的醫療模式轉向一種整合深層衰老生物標記的預防性模型。像是 InsideTracker 和 Singulomics 這樣的個人化醫療平台,利用人工智慧(AI)結合血液生物標記、DNA 資料和生理指標,以制定個別化的延壽策略。毫無疑問,衰老研究領域正蓬勃發展。我不敢預測可持續“徹底延壽”的首個案例將來自何處,但我認為這很可能在未來幾年內實現,而不是數十年。無論你是研究者、投資者還是像我一樣的科學部落客,這都是一個值得關注和參與的有趣領域。那麼,對於“一般人”而言,我們現在該怎麼做呢?在“所有強大技術仍在小鼠身上進行測試”的當下,我們可以考慮一些具體措施。例如,“超越單一生物標記的整合性策略”,我們應該探索多組學整合與動態監測如何應用於延緩衰老。僅依賴單一生物標記(如端粒長度或炎症指標)顯得過於簡化;專家們更關注的是多組學整合分析(multi-omics integration),即結合基因組學、轉錄組學、蛋白質組學及代謝組學等資料,以全面理解個體衰老的複雜機制。
動態監測至關重要。單次檢測只能提供某一時間點上的快照,而持續追蹤生物標記值變化趨勢則能更準確地評估幹預措施效果並調整個人化策略。因此,未來延壽醫療將重點放在持續性的健康管理平台上,提供動態資料追蹤、預測和幹預建議,而非一次性的檢測與建議。
“超越單純延長壽命:聚焦健康壽命提升及細胞衰老目標治療”也日益受到重視。延壽研究不僅僅要延長生命,更重要的是提升健康壽命,即增長健康且無疾病生活年份。目前研究重點已從單純延長生命轉向減緩與遲滯衰老相關疾病,如心血管病、神經退行性疾病和癌症等。作為衰老關鍵驅動因素之一的細胞衰老,也成為了重要研究目標。
隨著對抗衰老治療方法的不斷深入,例如針對細胞衰老進行靶向消除(Senolytics)的初步臨床結果顯示其潛力巨大,但精準瞄準受損細胞而避免正常細胞受損仍然是一項重大挑戰。同時,其他針對線粒體功能障礙及蛋白質錯誤摺疊等相關途徑的靶向治療也在積極開發中。在這樣充滿希望與挑戰的新興領域中,每一步都值得期待與觀察。
抗衰老新療法:雷帕黴素以外的突破性研究
當前已知有一些可行用的藥物顯示出抗衰老效果,其中一個很好的例子是雷帕黴素(rapamycin)。不過,如我之前所提,我認為這並不適合像我這樣的「普通人」。雖然從技術上來說,我的專業確實使我能夠深入理解這些分子及其潛在的益處與風險(不敢自誇,但畢竟我是化學博士),但目前我還不準備進入這個深奧的領域。尤其是在我目前居住的國家,醫療系統可能讓追蹤生物標記和試驗延緩衰老藥物變得相當具有挑戰性。事實上,例如雷帕黴素,由於其潛在的毒性和免疫抑制效應,通常並不適合一般使用。我無法推薦自己在此年齡下且仍相對健康時會選擇的不建議使用之物。或許等到我六十或七十歲時,我會更主動且大膽地嘗試調整我的分子途徑,但希望到了那時我們能有一套更清晰、更簡單的最佳實踐!
**專案1:超越雷帕黴素:聚焦Senolytics與Senomorphics的協同作用及個別化治療策略**
儘管雷帕黴素在延緩衰老方面展現出潛力,其免疫抑制副作用限制了其廣泛應用。現今抗衰老研究已超越單一藥物,積極探索Senolytics(清除衰老細胞)與Senomorphics(抑制衰老細胞分泌有害物質)的協同作用。這兩類藥物機制不同,聯合使用可能產生更顯著的抗衰老效果,同時減少單一藥物的不良反應。
**深入要點:** 針對不同衰老表型(例如心血管疾病、神經退行性疾病等)發展個別化治療方案至關重要。透過高通量篩選技術結合多組學分析,可以精確識別個體特徵,從而選擇最有效的Senolytics和Senomorphics組合並調整劑量,以最大化療效並將副作用降至最低。
**專案2:利用CRISPR-Cas技術進行衰老相關基因編輯的可能性與挑戰**
基因編輯技術,特別是CRISPR-Cas系統,為精準操控衰老相關基因提供了前所未有的機會。透過靶向與端粒長度維持以及DNA損傷修復相關的重要基因,我們可以期望延緩甚至逆轉衰老過程。
**深入要點:** 在抗衰老治療中運用CRISPR-Cas技術仍面臨巨大挑戰,包括脫靶效應、效率和特異性的考量,以及倫理道德問題。因此,需要大量基礎研究以了解複雑且多因素影響下的衰老機制,以開發更安全、有效的方法。在未來研究中,也許會看到更加精確的基因編輯方式,以及人工智慧輔助設計的新策略。
值得注意的是,在關注新興科技如CRISPR及其對於延緩或逆轉生理退化之潛力時,我們也必須慎重評估其帶來的新挑戰及風險。在科學探索的大潮中,希望我們能找到既安全又有效的方法,使每個人都能享受到更健康、更長壽的人生。
對於當今普通人來說,更實際的做法可能是專注於一些安全的生活方式幹預,例如運動、飲食調整(例如,卡路里限制或間歇性禁食)、保持良好的睡眠、定期進行健康檢查,以及一些天然補充品,如 spermidine、NAD+ 前體或 urolithin-A,這些選擇在安全性上更具保障且更容易融入日常生活。儘管如此,即使是補充品也並非如人們所想那樣無害,因此您必須諮詢醫生……或者,我不知道,也許可以找 Bryan Johnson?無論如何,這不是醫療建議。我不是醫學博士,而是一名化學博士。
參考來源
2024亞太精準抗衰老醫學大會
聚焦: AI 3D面部衰老檢測 IV 注射NAD+、NMN抗衰老 中醫抗衰老地圖,中西醫臨床應對策略,前沿生物技術等。 提倡中西醫學并重和雙向融合,科學與臨床實踐 ...
來源: 臺灣中西整合醫學會美國生技公司運用AI 找出能殺死老化細胞的抗衰老藥物
... AI可以如何被應用於醫學中,使科學家找出解決衰老的更有效療法。未來,研究團隊也將持續應用此AI 模型,推動抗衰老、長壽等領域的相關研究。 新聞來源 1. Ten Bridge ...
來源: 科學月刊抗衰老藥物發展近況 - OUTLOOK 科技發展觀測平台
... 抗衰老藥物研發平台,利用這些先進的平台,能更有效率的研究各種抗衰老療法。 (5) 新診斷技術結合生物標誌物與AI技術,能透提升診斷技術的精準度及衰老速度的預測能力。
來源: OUTLOOK 科技發展觀測平台亞太精准抗衰老醫學會與印尼Natasha醫療集團聯手共啓 ...
基于這些發現,APPAM開發了一系列抗衰老藥物和治療方法,包括細胞治療、基因治療等,爲延緩衰老提供了全新的思路和手段。這些治療方法不僅能够有效改善老年 ...
來源: 奇摩新聞《國際要聞》Insilico Medicine以AI聚焦找出老化相關疾病的新藥靶點
週二發表在《Aging》期刊上的新研究描述了Insilico的PandaOmics軟體如何能夠預測新藥的分子靶點,以治療衰老和年齡相關的疾病,如阿茲海默症、帕金森氏症、 ...
來源: 國家新創獎仁人醫療領航先行AI精準運動復能抗衰健康老
用AI智慧化運動設備介入規律運動提供的精準運動成效極佳,已獲國民健康署研究證實,發展不同行動功能的運動模式,介入組經過16周運動後,健康高齡者高達2成明顯改善 ...
來源: Ankecare 創新照顧开创康寿新时代抗衰新策略已在涌现
代谢组学+AI技术,能够早于临床前预警患病风险,还可以量化衰老/疾病风险。“人工智能已在多行业多方面进行应用。例如心梗、银发经济已经在保险公司中应用。
來源: 中国医院院长AI也會選新藥! 人工智慧挑出3種傳統中藥可以抗衰老
蘇格蘭愛丁堡大學的研究團隊開發模擬系統,藉由已知的研究成果,訓練AI來幫忙尋找有效的抗衰老藥,最後發現3種傳統中藥內化學物質可抗衰老.
來源: 全球醫療採購網

 全部
全部 康健
康健
相關討論